Газова смес и състава
Модели разисквано по-горе, дадени за газове, които са чисти вещества, т.е. в което всички молекули са еднакви.
Използваната техника не само чисти газове, но също така и смес от чисти газове (например въздух, състояща се от азот и кислород, азот-водород смес, и т.н.).
Газ smes- механична смес от газове, всеки от които е предмет на законите на идеалните газове.
Сместа реагират химически. Запазване на химичния им идентичност. Газовите смеси са, например, атмосферен въздух или горивни продукти в котли горене устройства и пара, двигатели с вътрешно горене и газови турбини. Тези смеси са по-специално азот, въглероден двуокис, серен двуокис, водна пара и кислород.
Особен случай на газови смеси е смес от идеалните газове. Познаването на поведение на идеалната газова смес позволява да се опише поведението на смес от реални газове.
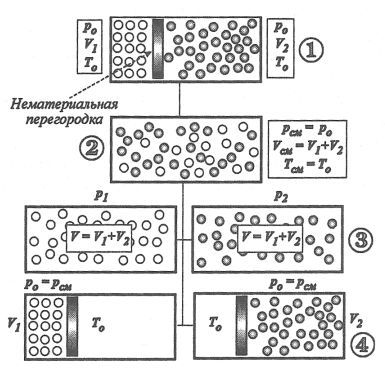
Фиг. 1.1.11 Определяне даден (частичен) налягане и обем на газ сместа компоненти
Нека да разберете какво се нарича частичен (намален) са в размер на компонент. Напълнете бутилката с две различни газове, те се отделят напълно фин (не-материал) стена (фиг. 1.1.11).
Под действието на налягането на газа в лявата и дясната страна дял е установен в междинна позиция, в която налягането на газа към него, както наляво и надясно - са еднакво. Нека двете газове са същите температура T0 (състояние 1; ris.1.1.11). Всяка от газовете на равни налягания и температури ще заемат V1 и V2 обем.
Премахване перце града. Газовете се смесват (условие 2). Налягането и температурата на газовата смес не се променя, т.е.. E.
Всяка от газа в това състояние ще заемат общия обем, т.е. този, който те заета преди смесване VCM = V 1 + V 2.
Сега ние ще се обърне за да се отстранят от цилиндъра на двата газа. Контейнерът ще остане друг газ, който ще заемат общ обем V = VCM (състояние 3).
Във всеки от тези случаи налягането на газа в цилиндъра пада от P0 = RCM на Р1 или Р2 (както преди, заета от газ по протежение на целия обем на контейнера, и сега заема същото количество газ всеки поотделно). Запазване на всеки от възможните начини за всеки отделен температура на газа в цилиндъра, температура на равни техни смеси SCI. По този начин, всеки от газовете отделно при температура Т1 = Т2 = SCI и екран VCM = V 1 + V 2. ще създаде налягане Р1 или Р2
Налягането, което ще създаде всяка от газовата смес индивидуално (други газове отстранени) в същия обем, както преди цялата смес се проведе и при условие, че температурата е равна на температурата на сместа, Т1 = Т2 = SCI. nazyvaetsyapartsialnym (намалено) налягане.
Основният закон на поведението на смес идеален газ е закон на Далтон. твърди, че всеки отделен газ в сместа се държи като, ако е при температура на сместа, един е на целия обем на сместа.
Всяка от газовете, образуващи сместа има на стената на съда под налягане, наречено парциално налягане. Разположен обем равен обем смес от всеки от газовете, представляващи смес е под неговото парциално налягане и температура на сместа.
газ под налягане смес се равнява на сумата Dalton закона на частични налягания:
За определяне количества характеризиране на газова смес, е необходимо да се знае състава на газа. Тя се определя от количеството на всеки от газовете в сместа, и се определя от теглото или обема.
За да се определи точно съставът на сместа с помощта на маса и обем фракции:
Мас фракция на газ навлиза сместа е съотношението на масата му към общото тегло на сместа.
масовите части на компонентите на газовата смес, са определени:
Молекули на всеки газ навлиза сместа се равномерно разпределени по целия обем, така че всеки от газовете, съставляващи сместа се разпределя равномерно по целия обем и заема същия обем, както и цялата смес.
За да се установи обемната фракция на компонент въвежда концепцията за частичен компонент обем.
Сега, с газовете протичат друго. Всяка от газовата смес се намалява с дял поотделно, преди да се създаде налягане със смес от тези газове в пълен екран цилиндър, т.е. в състояние 2. Когато сгъстен повишаване на температурата газ и следователно бутилката ще се охлажда, като по този начин постигане на постоянството всяка температура на газа , Важно е, че газът се компресира, температурата остава при температура на газовата смес, т.е. Т = Т1 = Т2 = SCI (състояние 4).
По този начин, всеки поотделно газ при налягане и температура, равна на налягането и температурата на сместа от P = Р1 = Р2 = PCM газ. Т = Т1 = Т2 = SCI. ще заема определен обем (V1, съответно, или V 2).
Това се нарича частичен обем (намаляване) на обема.
Obomomkomponenta нарича частичен обем, който ще заемат при температурата и налягането на сместа.
Очевидно е, че в този пример, частични (редуциран) обеми газ са техния обем преди смесване V 1 и V 2.
Ако газовата смес се състои от п газове е маркиран с
количества от компонентите на сместа чрез V 1. V 2, .... Vn и обемът на сместа чрез V см. След
обемната фракция на всеки компонент на газовата смес е съотношението на неговия частичен обем към обема на цялата смес.